Gebaseerd op de eerdere ‘levende robots van kikkercellen’ (xenobots), verlegde het wetenschappelijke onderzoeksteam van het Wyss Institute van Tufts University en Harvard University opnieuw de grenzen van bio-engineering en creëerde een nieuwe miniatuur levende machine met een eigen zenuwstelsel – ‘neurobots’. Het demonstreerde zelfgeorganiseerde neurale netwerken en complexere gedragspatronen, wat een nieuw venster bood om te begrijpen hoe organismen functionele structuren bouwen.
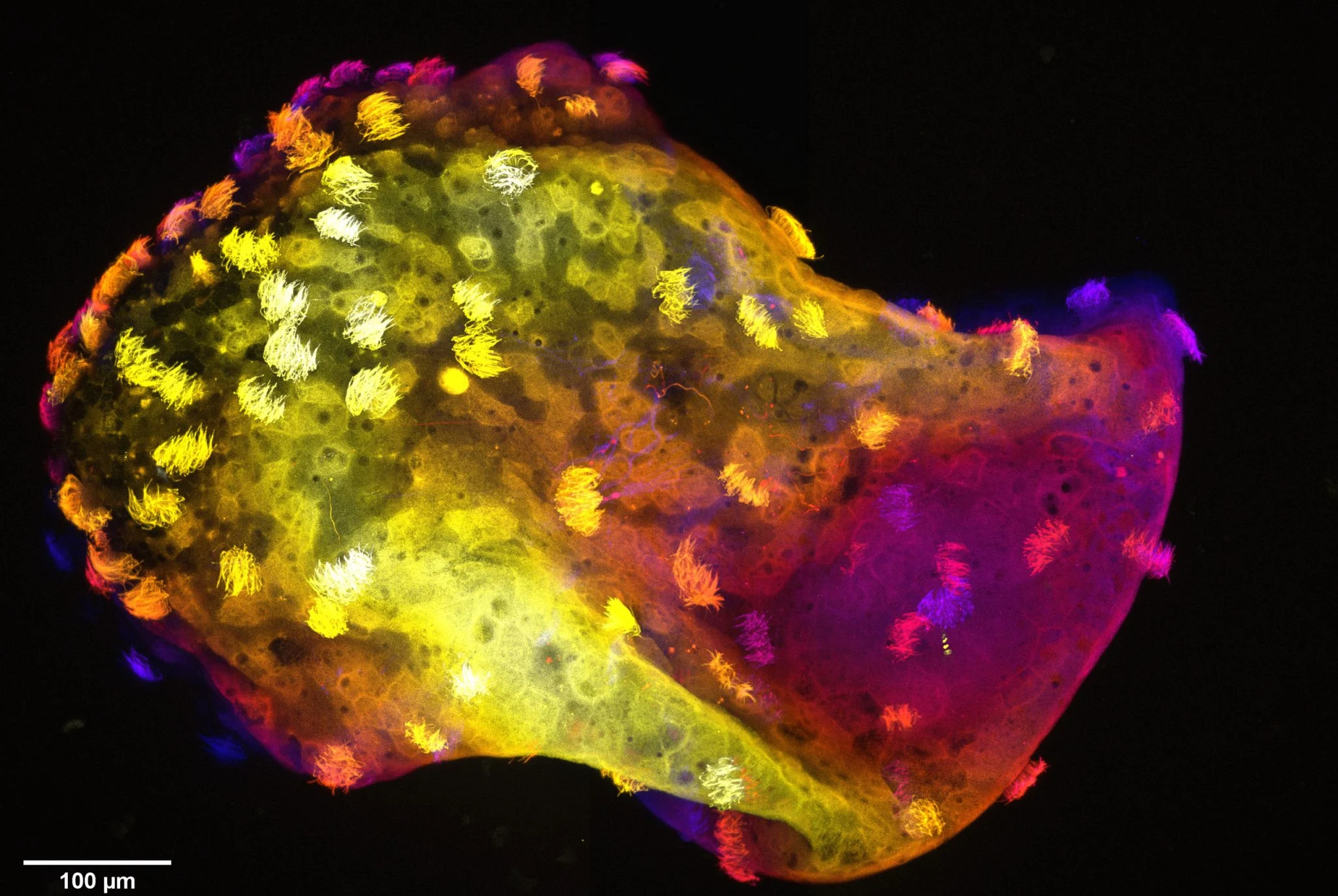
Al in 2020 gebruikten onderzoekers van Tufts University embryonale cellen van Xenopus laevis om "robotachtige" biologische structuren op micronschaal te bouwen: kikkercelrobots. Ze kunnen zich in het water bewegen, zichzelf repareren en zelfs verspreide cellen verzamelen om nieuwe individuen te genereren. De structuren, die zichzelf volledig uit levende cellen samenstellen, zonder steigers of genetische modificatie, leven ongeveer 9 tot 10 dagen en zijn voor hun overleving afhankelijk van voedingsstoffen die zijn opgeslagen in de oorspronkelijke embryonale cellen. Op basis hiervan heeft het onderzoeksteam onderzocht: wat zou er gebeuren als deze levende structuren zouden worden ‘uitgerust’ met zenuwstelsels?
In het laatste onderzoek hebben wetenschappers een groep neurale voorlopercellen geïmplanteerd die zich zullen ontwikkelen tot neuronen tot een biologische robot in aanbouw om een zogenaamde 'neurobot' te vormen. Deze cellen worden ingebed in het korte tijdsbestek waarin het bolvormige weefsel zich nog in de vroege ontwikkelingsstadia bevindt, en worden dan geleidelijk volwassen, groeien dendrieten en axonen en strekken zich uit naar het binnenste en het oppervlak om een eenvoudig en compleet neuraal netwerk op te bouwen. Relevante resultaten zijn onlangs gepubliceerd in het tijdschrift Advanced Science.
Het project, mede geleid door Michael Levin, hoogleraar biologie van Vannevar Bush aan de Tufts University, en Haleh Fotowat van het Wyss Institute, maakt deel uit van een grotere onderzoeksinspanning om te begrijpen hoe groepen cellen zichzelf organiseren in complexe structuren in onbekende omgevingen. Onderzoekers hopen dat dit soort ‘from scratch’-systemen de basisregels voor de vorming en vormgeving van het zenuwstelsel kan onthullen, en daarmee een theoretische basis kan bieden voor synthetische biologie en regeneratieve geneeskunde, die kunnen worden gebruikt om in de toekomst nieuwe biologische structuren te ontwerpen of beschadigde weefsels te herstellen.
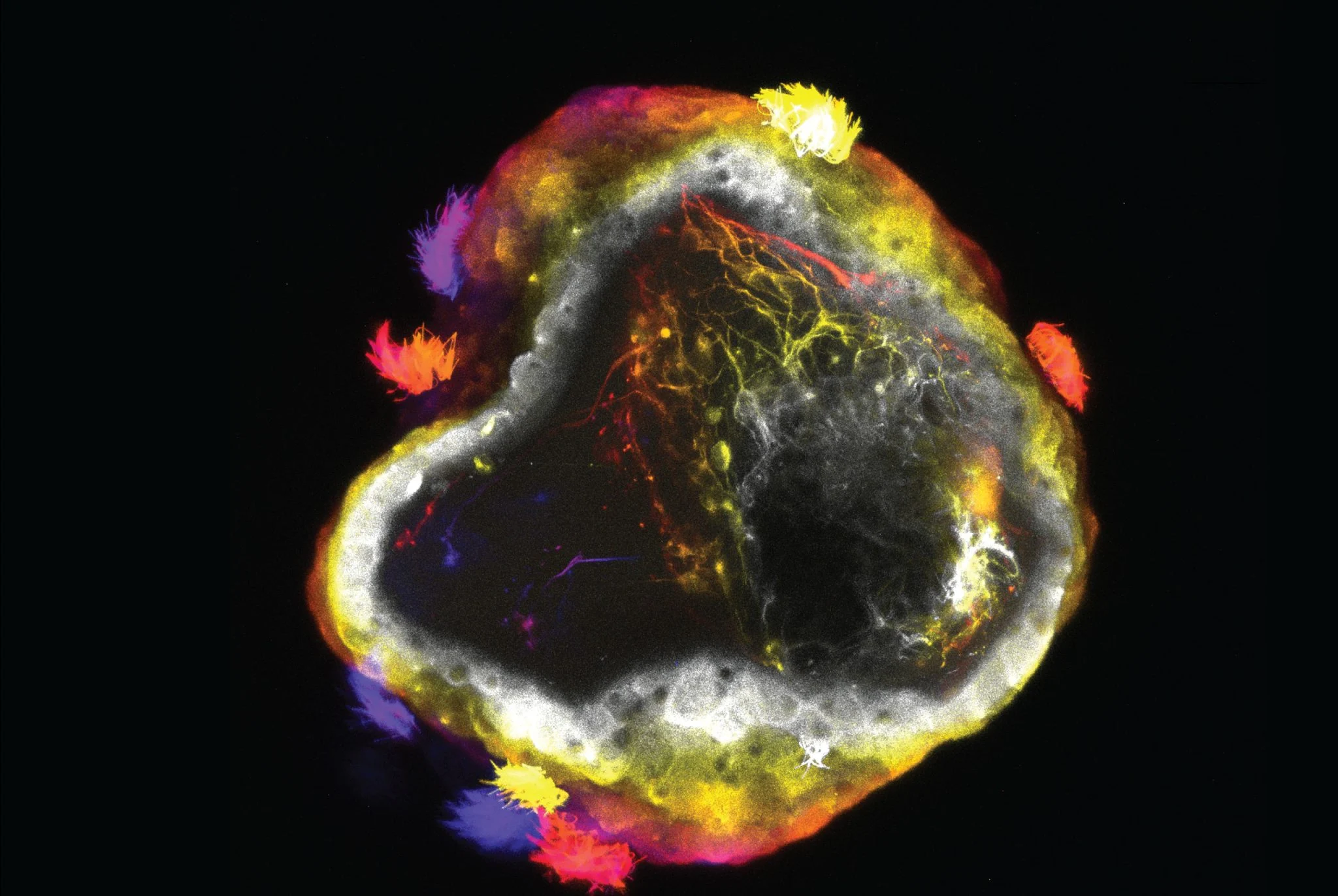
In specifieke experimenten isoleerde het team eerst voorloperhuidcellen uit vroege Xenopus-embryo's. Deze cellen aggregeren op natuurlijke wijze tot kleine bolvormige structuren in een kweekschaal en hun oppervlakken zijn bedekt met dichte cilia (cellen met meerdere trilharen). Door de gecoördineerde beweging van de cilia kan de originele "kikkercelrobot" in het water zwemmen. Na het toevoegen van neurale voorlopercellen aan deze basis, heeft de gevormde "neurobot" zijn vorm aanzienlijk veranderd in vergelijking met het verleden, en is hij in het algemeen groter en slanker geworden.
Microscopische observatie toonde aan dat deze ingebedde neuronen niet alleen typische dendritische en axonale structuren ontwikkelden, maar ook synaps-gerelateerde eiwitmarkers tot expressie brachten, wat aangeeft dat verbindingen tussen cellen tot stand waren gebracht en in staat waren tot signaaloverdracht. Door middel van calciumbeeldvormingstechnologie bevestigden de onderzoekers verder dat de neuronen in de neurorobot in staat zijn tot elektrische activiteit en een vereenvoudigd functioneel neuraal netwerk vormen.
De toevoeging van zenuwstelsels verandert ook aanzienlijk het gedrag van deze levende machines. Vergeleken met biologische robots zonder neuronen, hebben neurorobots frequentere algemene activiteiten en complexere bewegingstrajecten, waarbij ze repetitieve bewegingspatronen vertonen in plaats van eenvoudige rechte lijnen of willekeurige wandelingen. Om de rol van neurale activiteit in gedrag te testen, gebruikte het team pentyleentetrazol, een medicijn waarvan bekend is dat het de hersenactiviteit beïnvloedt en epileptiforme reacties opwekt, en observeerde het effect ervan op de beweging van deze levende structuren. De resultaten laten zien dat het medicijn de bewegingspatronen van neurorobots op een heel andere manier verandert dan op biologische machines die geen neuronen bevatten, wat erop wijst dat nieuw gevormde neurale netwerken actief het gedrag van deze ‘machines’ vormgeven.
Fotovat zei dat dit werk niet alleen bedoeld is om een "controle-eenheid" aan de biologische robot toe te voegen, maar nog belangrijker, om de interne principes van de vorming van het zenuwstelsel om te keren. Ze wees erop dat, vergeleken met het volgen van hoe neuronen deelnemen aan de productie van gedrag bij volwassen dieren zoals de zebravis, neurorobots een platform bieden om zenuwstelsels ‘vanaf nul’ op te bouwen, zodat we ons kunnen afvragen: ‘Plaats neuronen in een volkomen ongekende situatie, welke aangeboren regels zullen ze in netwerken organiseren volgens?’
Levine benadrukte dat neurorobotica een unieke kans biedt om te bestuderen “hoe neurale netwerken beweging en gedrag beïnvloeden in een systeem met een lichaam.” In traditionele experimentele modellen hebben het lichaam en het zenuwstelsel vaak een lange geschiedenis van co-evolutie meegemaakt, terwijl neurorobots een geheel nieuwe combinatie zijn zonder evolutionaire achtergrond, die helpt leer- en evolutionaire factoren los te laten en intuïtief te observeren hoe cellen en netwerken samenwerken in fysieke structuren.
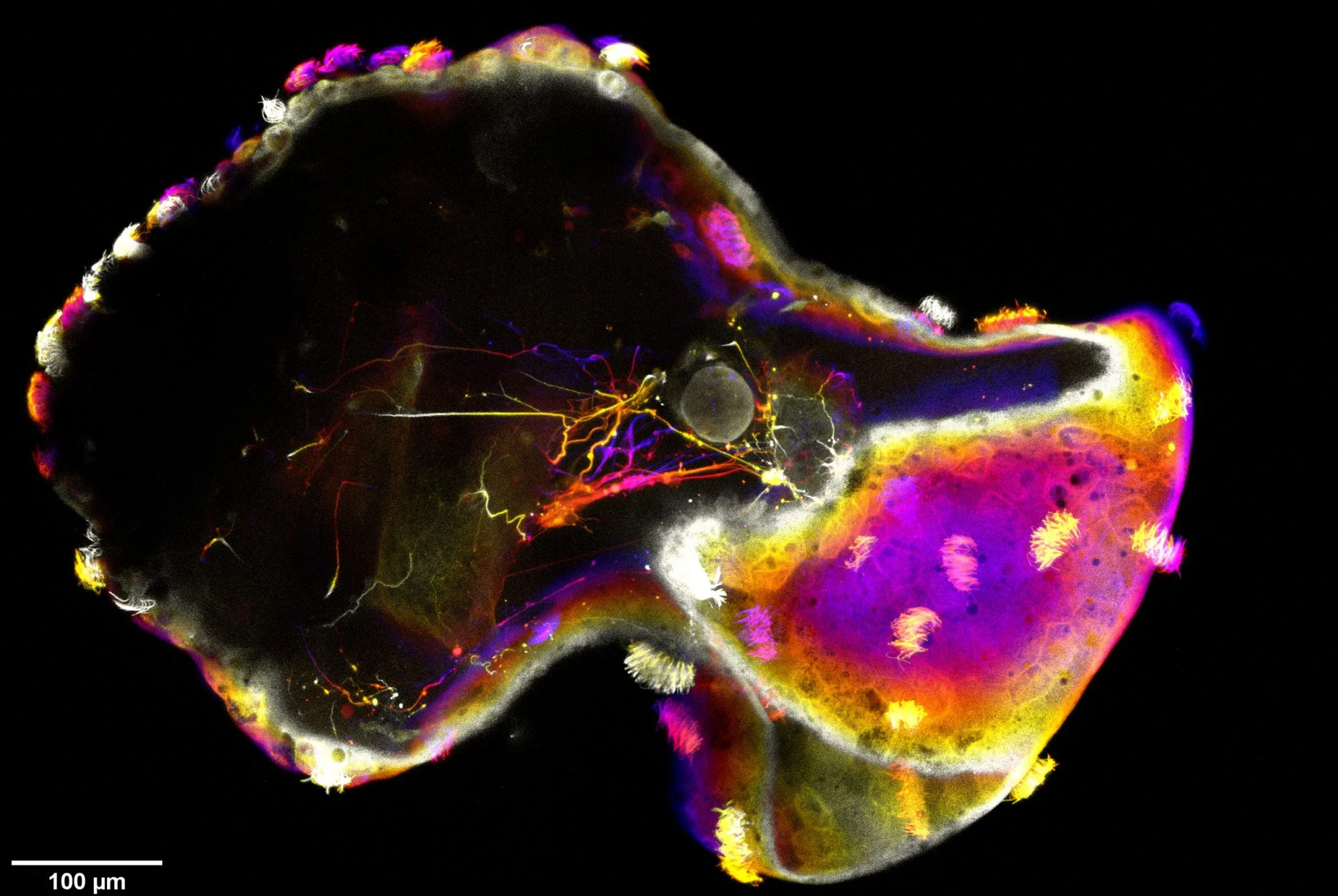
Naast morfologische en gedragsveranderingen ontdekten de onderzoekers ook onverwachte genexpressiepatronen in de neurobots. Naast genen die verband houden met belangrijke hersenreceptoren, ontdekte het team ook de activering van een aantal genen die betrokken zijn bij visuele verwerking, waaronder genen die normaal tot expressie komen in lichtgevoelige cellen in het oog. Dit betekent dat als de levensduur verder wordt verlengd en de kweekomstandigheden worden geoptimaliseerd, neurorobots in de toekomst het vermogen kunnen ontwikkelen om op licht te reageren.
Levin stelde een toekomstgerichte hypothese voor: deze neurorobots kunnen bepaalde genmodules die nuttig zijn voor potentiële toekomstige functies "pre-upreguleren", ter voorbereiding op de daaropvolgende functionele evolutie. "Als ze langer leven, zullen ze dan echte fotoreceptoren verder ontwikkelen?" Hij zei dat dit een vraag is die het team momenteel actief onderzoekt.
De onderzoekers wezen erop dat om "volledig nieuwe dingen te bouwen" met biologische materialen, je eerst moet begrijpen hoe cellen zelf problemen oplossen en "beslissingen" nemen in onbekende omgevingen. Neurorobots zijn zo'n experimenteel platform: ze hebben geen gevestigde ontwikkelingsprogramma's en geen structurele sjablonen achtergelaten door natuurlijke selectie, maar ze tonen nog steeds het vermogen om zichzelf te organiseren, netwerken te vormen en gedrag te genereren. Dit daagt niet alleen ons traditionele begrip van de grens tussen ‘lichaam’ en ‘zenuwstelsel’ uit, maar opent ook de verbeelding voor toekomstige programmeerbare levende systemen, zoals zelfherstellende micro-medische apparaten en intelligente weefselmanipulatiecomponenten.